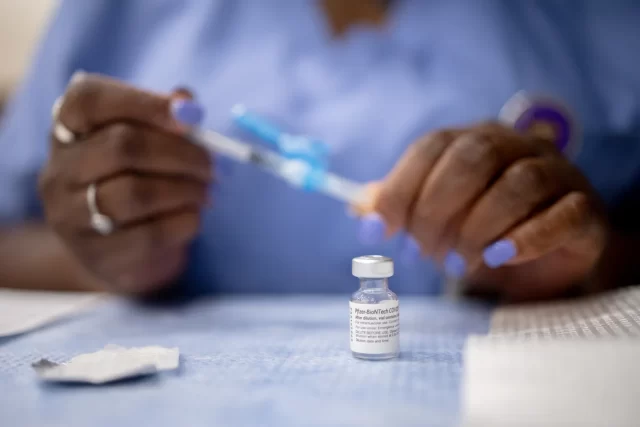
سازمان غذا و دارو آمریکا (FDA) تأیید کامل واکسن کووید-۱۹ فایزر را که یکی دیگر از نشانه های مهم در کمپین ایمن سازی است، صادر کرده است. این واکسن قبلاً برای افراد بالای ۱۲ سال در ایالات متحده تحت مجوز استفاده اضطراری در دسترس بود اما در حال حاضر، مجوز رسمی آن در ایالات متحده، صادر شده است.
با تأیید کامل و نهایی، Pfizer و BioNTech می توانند واکسن کووید-۱۹ خود را مستقیماً به مصرف کنندگان عرضه کنند. واکسن با نام Comirnaty برای افراد بالای ۱۶ سال به بازار عرضه می شود.
واکسن کووید-۱۹ فایزر همچنان تحت مجوز استفاده اضطراری برای افراد ۱۲ تا ۱۵ ساله در دسترس خواهد بود. جانت وودکاک، سرپرست FDA، در بیانیه ای گفت:
“تأیید FDA برای این واکسن یک نقطه عطف است زیرا ما در حال مبارزه با همه گیری بیماری کرونا هستیم و باید به آن ادامه دهیم. در حالی که این واکسن و دیگر استانداردهای دقیق و علمی FDA برای مجوز استفاده اضطراری به عنوان اولین واکسن تأیید شده این بیماری توسط FDA مطابقت دارند، عموم مردم می توانند بسیار مطمئن باشند که این واکسن از استانداردهای بالای ایمنی، اثربخشی و تولید برخوردار است؛ از این رو توانسته کیفیت مورد نیاز FDA برای یک محصول تأیید شده را یه دست آورد.”
صدور این تاییدیه ممکن است شرکت ها و مدارس بیشتری را مجبور به انجام واکسیناسیون کند. در حالی که انجام واکسیناسیون تحت مجوز اضطراری برای آن ها قانونی است، برخی از آنان تمایلی به انجام این کار ندارند. مقامات بهداشت عمومی امیدوارند که این تأیید کامل افراد بیشتری را به واکسیناسیون ترغیب کند.
شرکت های داروسازی باید تا شش ماه اطلاعات ایمنی و اثربخشی واکسن خود را به FDA ارائه دهند تا بتوانند درخواست خود را برای کسب مجوز بیولوژیکی ثبت کنند. این آژانس فقط از شرکت ها خواسته است تا دو ماه اطلاعات را قبل از درخواست مجوز استفاده اضطراری جمع آوری کنند. زمان بندی کوتاه شده به آژانس اجازه می دهد تا از برخی مراحل قانونی طولانی تر بگذرد و واکسن ها را به سرعت در طول بحران به مردم برساند.
تأیید FDA ممکن است به برخی از افرادی که در مورد واکسیناسیون شک و تردید داشتند، کمک کند. یک نظرسنجی در ماه مه نشان داد که یک سوم بزرگسالان واکسینه نشده در صورت تایید شدن یک واکسن کووید-۱۹، اقدام به دریافت آن خواهند کرد.
اکنون که یک واکسن کرونا به صورت تأیید کامل شده است، سایر شرکت های دارویی نمی توانند از FDA مجوزهای جدید استفاده اضطراری را بخواهند. مجوزهای اضطراری فقط در صورتی که گزینه های تأیید شده ای در دسترس نباشد، برای داروها یا واکسن ها صادر می شود.
اکنون که مجوز واکسن کووید-۱۹ فایزر صادر شده است، دیگر واکسن اضطراری در دسترس نخواهد بود. به عنوان مثال، اگر AstraZeneca بخواهد واکسن خود را در ایالات متحده در دسترس قرار دهد، باید با فرایند تأیید رسمی طولانی تر شروع کند.